Пептидтер - пептидтік байланыстар арқылы көптеген аминқышқылдарының қосылуы нәтижесінде түзілетін қосылыстар класы.Олар тірі организмдерде барлық жерде кездеседі.Осы уақытқа дейін тірі организмдерден ондаған мың пептидтер табылды.Пептидтер әртүрлі жүйелердің, мүшелердің, ұлпалардың және жасушалардың функционалдық әрекеттерін реттеуде және тіршілік әрекетінде маңызды рөл атқарады және көбінесе функционалдық талдауда, антиденелерді зерттеуде, препараттарды жасауда және басқа салаларда қолданылады.Биотехнология мен пептидті синтездеу технологиясының дамуымен пептидті препараттардың саны артып, клиникада қолданыла бастады.
Пептидтік модификациялардың алуан түрлілігі бар, оларды жай ғана модификациядан кейінгі және процесті модификациялау (алынған амин қышқылы модификациясын қолдану) және N-терминал модификациясы, C-терминал модификациясы, бүйірлік тізбек модификациясы, аминқышқылдарының модификациясы, қаңқа модификациясы, т.б., модификациялау орнына байланысты (1-сурет).Негізгі тізбек құрылымын немесе пептидтік тізбектердің бүйірлік тізбек топтарын өзгертудің маңызды құралы ретінде пептидті модификациялау пептидтік қосылыстардың физикалық және химиялық қасиеттерін тиімді өзгертуге, суда ерігіштігін арттыруға, in vivo әсер ету уақытын ұзартуға, олардың биологиялық таралуын өзгертуге, иммуногенділікті жоюға мүмкіндік береді. , токсикалық жанама әсерлерді азайту және т.б. Бұл мақалада пептидтерді өзгертудің бірнеше негізгі стратегиялары және олардың сипаттамалары енгізілген.
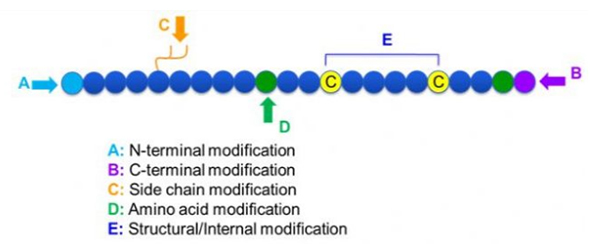
1. Циклизация
Циклдік пептидтердің биомедицинада қолдануы көп, ал биологиялық белсенділігі бар көптеген табиғи пептидтер циклдік пептидтер болып табылады.Циклдік пептидтер сызықтық пептидтерге қарағанда қаттырақ болғандықтан, олар ас қорыту жүйесіне өте төзімді, ас қорыту жолында өмір сүре алады және мақсатты рецепторларға көбірек жақындық көрсетеді.Циклизация циклдік пептидтерді синтездеудің ең тікелей әдісі болып табылады, әсіресе үлкен құрылымдық қаңқасы бар пептидтер үшін.Циклизация режимі бойынша оны бүйірлік тізбекті-бүйірлік тізбекті типке, терминалды - бүйірлік тізбекті типті, терминалды - терминалды типті (ұшты-ұшты типті) бөлуге болады.
(1) бүйірлік тізбектен бүйірлік тізбекке
Бүйірлік тізбектен бүйірлік тізбекке циклденудің ең көп таралған түрі цистеин қалдықтары арасындағы дисульфидті көпір болып табылады.Бұл циклизация жұп цистеин қалдықтарының қорғанышсыздануымен, содан кейін дисульфидті байланыстарды қалыптастыру үшін тотығуымен енгізіледі.Полициклді синтезге сульфгидрилді қорғау топтарын таңдап алып тастау арқылы қол жеткізуге болады.Циклизацияны диссоциациядан кейінгі еріткіште де, диссоциацияға дейінгі шайырда да жасауға болады.Шайырлардағы циклизация еріткіштің циклизациясына қарағанда тиімділігі төмен болуы мүмкін, өйткені шайырлардағы пептидтер циклденген конформацияны тез түзбейді.Бүйірлік тізбектің тағы бір түрі – бүйірлік тізбек циклизациясы аспартин қышқылы немесе глутамин қышқылының қалдығы мен негіздік амин қышқылы арасында амидтік құрылымның түзілуі болып табылады, ол бүйірлік тізбекті қорғау тобын полипептидтен таңдаулы түрде жою мүмкіндігін талап етеді. шайырда немесе диссоциациядан кейін.Бүйірлік тізбектің үшінші түрі – бүйірлік тізбектің циклизациясы тирозинмен немесе р-гидроксифенилглицинмен дифенил эфирлерінің түзілуі.Табиғи өнімдердегі циклизацияның бұл түрі тек микробтық өнімдерде кездеседі және циклизация өнімдері көбінесе әлеуетті емдік құндылыққа ие.Бұл қосылыстарды дайындау ерекше реакция жағдайларын қажет етеді, сондықтан олар әдеттегі пептидтердің синтезінде жиі қолданылмайды.
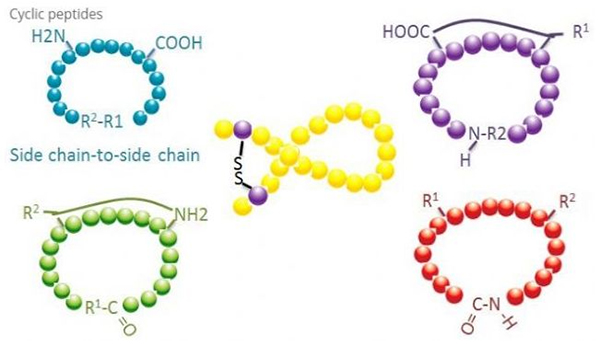
(2) терминалдан бүйірлік тізбекке
Терминалды бүйірлік тізбектің циклизациясы әдетте лизин немесе орнитин бүйірлік тізбегінің амин тобы бар C-терминалын немесе аспарагин қышқылы немесе глутамин қышқылының бүйір тізбегі бар N-терминалын қамтиды.Басқа полипептидтердің циклизациясы С терминалы мен серин немесе треонин бүйірлік тізбектері арасында эфирлік байланыстар құру арқылы жүзеге асырылады.
(3) Терминал немесе басынан құйрық түрі
Тізбекті полипептидтерді еріткіште айналдыруға немесе бүйірлік тізбекті циклациялау арқылы шайырға бекітуге болады.Пептидтердің олигомеризациясын болдырмау үшін еріткіштерді орталықтандыруда пептидтердің төмен концентрацияларын қолдану керек.Басынан құйрықты синтетикалық сақина полипептидінің шығымы полипептид тізбегінің реттілігіне байланысты.Сондықтан циклдік пептидтерді кең ауқымда дайындамас бұрын алдымен ықтимал тізбектелген қорғасын пептидтерінің кітапханасын жасау керек, содан кейін ең жақсы нәтижелер бар тізбекті табу үшін циклизациялау керек.
2. N-метиляция
N-метиляция бастапқыда табиғи пептидтерде пайда болады және сутегі байланыстарының түзілуін болдырмау үшін пептидтер синтезіне енгізіледі, осылайша пептидтерді биодеградацияға және клиренске төзімді етеді.N-метилденген аминқышқылдарының туындылары арқылы пептидтерді синтездеу ең маңызды әдіс болып табылады.Сонымен қатар, N-(2-нитробензол сульфонилхлорид) полипептидті-шайыр аралық өнімдерінің метанолмен Мицунобу реакциясын да қолдануға болады.Бұл әдіс құрамында N-метилденген аминқышқылдары бар циклдік пептидтік кітапханаларды дайындау үшін қолданылған.
3. Фосфорлану
Фосфорлану – табиғатта кең тараған посттрансляциялық модификациялардың бірі.Адам жасушаларында белоктардың 30%-дан астамы фосфорланған.Фосфорлану, әсіресе қайтымды фосфорлану көптеген жасушалық процестерді басқаруда маңызды рөл атқарады, мысалы, сигнал беру, гендердің экспрессиясы, жасушалық цикл мен цитоскелеттің реттелуі және апоптоз.
Фосфорлануды әртүрлі аминқышқылдарының қалдықтарында байқауға болады, бірақ фосфорланудың ең көп тараған нысандары серин, треонин және тирозин қалдықтары болып табылады.Фосфотирозин, фосфотреонин және фосфозерин туындылары синтез кезінде пептидтерге енгізілуі немесе пептидтік синтезден кейін түзілуі мүмкін.Селективті фосфорлануға серин, треонин және тирозин қалдықтары арқылы қол жеткізуге болады, олар қорғаныш топтарын таңдап алып тастайды.Кейбір фосфорлану реагенттері де полипептидке кейінгі модификация арқылы фосфор қышқылы топтарын енгізе алады.Соңғы жылдары лизиннің арнайы фосфорлануына химиялық селективті Штаудингер-фосфит реакциясы арқылы қол жеткізілді (3-сурет).
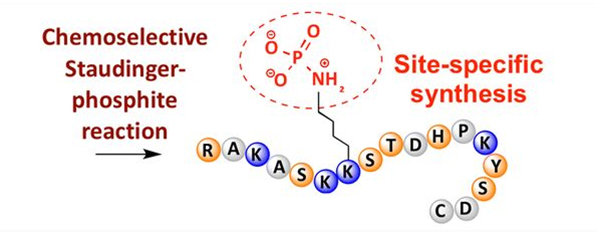
4. Миристойлану және пальмитойляция
N-терминалдың май қышқылдарымен ацилденуі пептидтердің немесе ақуыздардың жасуша мембраналарымен байланысуына мүмкіндік береді.N-терминалдағы миридамойлденген реттілік Src протеин киназалары мен кері транскриптаза Gaq протеиндерін жасуша мембраналарымен байланысуға бағыттауға мүмкіндік береді.Мирист қышқылы стандартты қосылу реакциялары арқылы шайыр-полипептидтің N-терминалымен байланыстырылды және алынған липопептид стандартты жағдайларда диссоциациялануы және RP-HPLC арқылы тазартылуы мүмкін.
5. Гликозилдену
Ванкомицин және тейколанин сияқты гликопептидтер дәріге төзімді бактериялық инфекцияларды емдеу үшін маңызды антибиотиктер болып табылады, ал басқа гликопептидтер иммундық жүйені ынталандыру үшін жиі қолданылады.Сонымен қатар, көптеген микробтық антигендер гликозилденгендіктен, инфекцияның емдік әсерін жақсарту үшін гликопептидтерді зерттеудің маңызы зор.Екінші жағынан, ісік жасушаларының жасушалық мембранасындағы ақуыздар анормальды гликозилдену көрсетеді, бұл гликопептидтерді қатерлі ісік пен ісік иммундық қорғаныс зерттеулерінде маңызды рөл атқарады.Гликопептидтер Fmoc/t-Bu әдісімен дайындалады.Треонин және серин сияқты гликозилденген қалдықтар көбінесе гликозилденген амин қышқылдарын қорғау үшін пентафторфенол эфирімен белсендірілген fMOC арқылы полипептидтерге енгізіледі.
6. Изопрен
Изопентадиенилдену С-терминалының жанындағы бүйірлік тізбектегі цистеин қалдықтарында жүреді.Протеин изопрені жасуша мембранасының жақындығын жақсарта алады және ақуыз-белок өзара әрекеттесуін қалыптастырады.Изопентадиенді ақуыздарға тирозинфосфатаза, кіші ГТаза, кохаперон молекулалары, ядролық ламина және центромерлі байланыстырушы ақуыздар жатады.Изопренді полипептидтерді шайырлардағы изопренді қолдану арқылы немесе цистеин туындыларын енгізу арқылы дайындауға болады.
7. Полиэтиленгликоль (ПЕГ) модификациясы
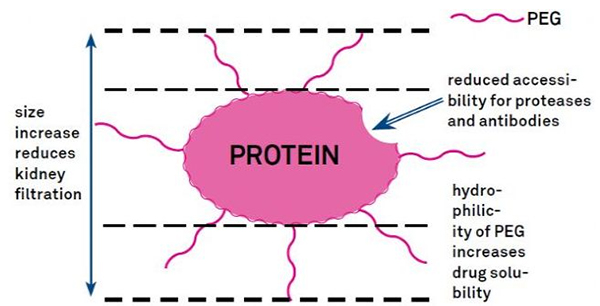
PEG модификациясын ақуыздың гидролитикалық тұрақтылығын, биотаралуын және пептидтердің ерігіштігін жақсарту үшін пайдалануға болады.Пептидтерге PEG тізбектерін енгізу олардың фармакологиялық қасиеттерін жақсарта алады, сонымен қатар протеолитикалық ферменттермен пептидтердің гидролизін тежейді.PEG пептидтері қарапайым пептидтерге қарағанда шумақтық капиллярлар қимасы арқылы оңай өтеді, бүйрек клиренсін айтарлықтай төмендетеді.PEG пептидтерінің in vivo белсенді жартылай шығарылу кезеңінің ұзаруына байланысты қалыпты емдеу деңгейін төменірек дозалар мен сирек пептидтік препараттармен сақтауға болады.Дегенмен, PEG модификациясының теріс әсерлері де бар.PEG көп мөлшері ферменттің пептидті ыдыратуына жол бермейді, сонымен қатар пептидтің мақсатты рецептормен байланысуын азайтады.Бірақ PEG пептидтерінің төмен аффинділігі әдетте олардың ұзағырақ фармакокинетикалық жартылай шығарылу кезеңімен өтеледі және денеде ұзағырақ болуы арқылы PEG пептидтерінің мақсатты тіндерге сіңу ықтималдығы жоғары болады.Сондықтан оңтайлы нәтижелер алу үшін PEG полимерінің спецификацияларын оңтайландыру керек.Екінші жағынан, PEG пептидтері бүйрек клиренсінің төмендеуіне байланысты бауырда жиналады, нәтижесінде макромолекулярлық синдром пайда болады.Сондықтан пептидтер есірткі сынағы үшін пайдаланылған кезде, PEG модификацияларын мұқият құрастыру қажет.
PEG модификаторларының жалпы модификациялық топтарын шамамен төмендегідей қорытындылауға болады: Амино (-амин) -NH2, аминометил-Ch2-NH2, гидрокси-ОН, карбокси-Ку, сульфгидрил (-тиол) -SH, малеймид -MAL, сукцинимид карбонаты - SC, сукцинимид ацетаты -SCM, сукцинимид пропионат -SPA, n-гидроксисукцинимид -NHS, акрилат-ch2ch2cooh, альдегид -CHO (мысалы, пропионал-алд, бутиРАЛД), акрил негізі (-акрилат-акрл), азидо-аз Биотин, флуоресцеин, глутарил -ГА, акрилатгидразид, алкин-алкин, р-толуэнсульфонат -ОТс, сукцинимид сукцинат -СС және т.б. Карбон қышқылдары бар PEG туындылары n-терминалды аминдермен немесе лизиннің бүйірлік тізбегімен біріктірілуі мүмкін.Амин белсендірілген PEG аспарагин қышқылына немесе глутамин қышқылының бүйірлік тізбектеріне қосылуы мүмкін.Зиянды белсендірілген PEG толық қорғалмаған цистеиннің бүйірлік тізбектерінің меркаптанымен конъюгациялануы мүмкін [11].PEG модификаторлары әдетте келесідей жіктеледі (ескерту: mPEG – метокси-ПЕГ, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) түзу тізбекті PEG модификаторы
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) екі функционалды PEG модификаторы
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) тармақталған PEG модификаторы
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Биотинизация
Биотин авидинмен немесе стрептавидинмен қатты байланысуы мүмкін, ал байланыс күші тіпті коваленттік байланысқа жақын.Биотинмен таңбаланған пептидтер әдетте иммундық талдауда, гистоцитохимияда және флуоресценция негізіндегі ағын цитометриясында қолданылады.Белгіленген антибиотикті антиденелер биотинленген пептидтерді байланыстыру үшін де пайдаланылуы мүмкін.Биотин жапсырмалары көбінесе лизиннің бүйірлік тізбегіне немесе N терминалына бекітіледі.6-аминокапрон қышқылы көбінесе пептидтер мен биотин арасындағы байланыс ретінде қолданылады.Байланыс субстратпен байланысуда икемді және стерикалық кедергі болған кезде жақсы байланысады.
9. Флуоресцентті таңбалау
Флуоресцентті таңбалауды тірі жасушалардағы полипептидтерді қадағалау және ферменттер мен әсер ету механизмдерін зерттеу үшін пайдалануға болады.Триптофан (Trp) флуоресцентті, сондықтан оны ішкі таңбалау үшін пайдалануға болады.Триптофанның эмиссиялық спектрі перифериялық ортаға байланысты және еріткіштің полярлығының төмендеуімен азаяды, бұл қасиет пептидтік құрылымды және рецепторлармен байланысуды анықтау үшін пайдалы.Триптофан флуоресценциясын протондалған аспарагин қышқылы мен глутамин қышқылымен сөндіруге болады, бұл оның қолданылуын шектейді.Дансил хлориді тобы (Dansyl) амин тобымен байланысқан кезде жоғары флуоресцентті болып табылады және көбінесе аминқышқылдары немесе ақуыздар үшін флуоресцентті белгі ретінде пайдаланылады.
Флуоресценциялық резонанстық энергияны түрлендіру (FRET) ферменттерді зерттеу үшін пайдалы.FRET қолданған кезде субстрат полипептидінде әдетте флуоресцентті таңбалау тобы және флуоресцентті сөндіру тобы болады.Белгіленген флуоресцентті топтар сөндіргішпен фотонды емес энергияны тасымалдау арқылы сөндіріледі.Пептид қарастырылып отырған ферменттен диссоциацияланған кезде, таңбалау тобы флуоресценция шығарады.
10. Торшалы полипептидтер
Торша пептидтерінде пептидті рецептормен байланысудан қорғайтын оптикалық алынбалы қорғаныс топтары бар.Ультракүлгін сәулеленуге ұшыраған кезде пептид белсендіріледі, оның рецепторға жақындығы қалпына келеді.Бұл оптикалық белсендіру уақытқа, амплитудаға немесе орынға сәйкес басқарылуы мүмкін болғандықтан, жасушаларда болатын реакцияларды зерттеу үшін торлы пептидтерді пайдалануға болады.Торлы полипептидтер үшін ең жиі қолданылатын қорғаныс топтары 2-нитробензил топтары және олардың туындылары болып табылады, олар пептидтік синтезде қорғаныш аминқышқылдарының туындылары арқылы енгізілуі мүмкін.Дамыған аминқышқылдарының туындылары лизин, цистеин, серин және тирозин болып табылады.Алайда аспартат пен глутамат туындылары пептидтердің синтезі мен диссоциациясы кезінде циклденуге бейімділігіне байланысты әдетте қолданылмайды.
11. Полиантигенді пептид (MAP)
Қысқа пептидтер әдетте иммунитетке ие емес және антиденелерді өндіру үшін тасымалдаушы ақуыздармен қосылуы керек.Полиантигенді пептид (MAP) лизин ядроларымен байланысқан бірнеше бірдей пептидтерден тұрады, олар жоғары потенциалды иммуногендерді спецификалық түрде көрсете алады және пептидті тасымалдаушы ақуыз куплеттерін дайындау үшін пайдаланылуы мүмкін.MAP полипептидтерін MAP шайырында қатты фазалық синтез арқылы синтездеуге болады.Дегенмен, толық емес қосылу кейбір тармақтарда пептидтік тізбектердің болмауына немесе кесілуіне әкеледі және осылайша бастапқы MAP полипептидінің қасиеттерін көрсетпейді.Балама ретінде пептидтерді бөлек дайындауға және тазартуға, содан кейін MAP-қа біріктіруге болады.Пептидтік ядроға бекітілген пептидтік тізбек жақсы анықталған және масс-спектрометриямен оңай сипатталады.
Қорытынды
Пептидтердің модификациясы пептидтерді жобалаудың маңызды құралы болып табылады.Химиялық түрлендірілген пептидтер жоғары биологиялық белсенділікті сақтап қана қоймай, сонымен қатар иммуногендік және уыттылық кемшіліктерін тиімді болдырмайды.Сонымен қатар, химиялық модификация пептидтерге жаңа тамаша қасиеттер бере алады.Соңғы жылдары полипептидтерді постмодификациялау үшін CH белсендіру әдісі қарқынды дамып, көптеген маңызды нәтижелерге қол жеткізілді.
Хабарлама уақыты: 20 наурыз-2023 ж
