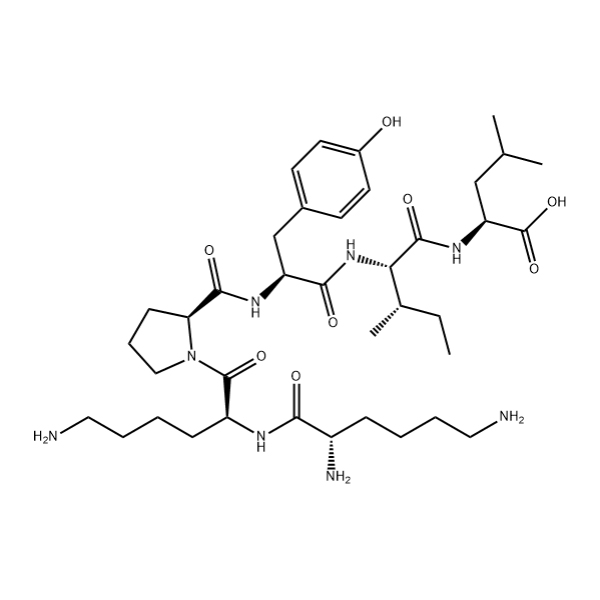
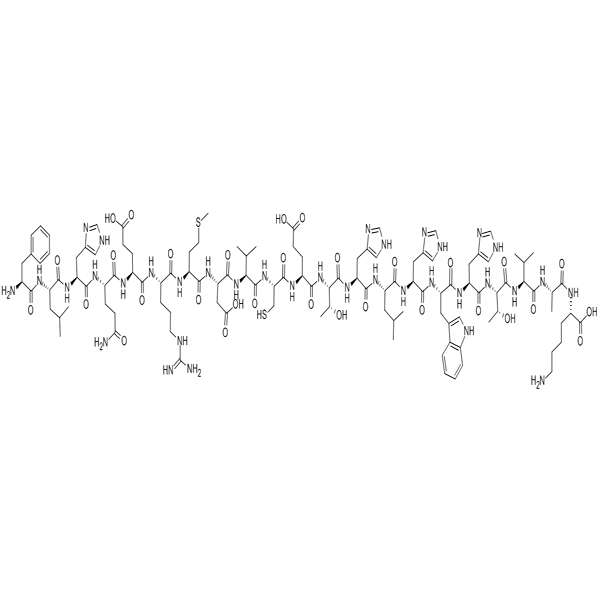
Раналексин/155761-99-2 /ГТ пептид/пептид жеткізушісі
Сипаттама
РаналексинРана пипиенс бақаларының тері бездері шығаратын пептидті антибиотик.Ол алғаш рет 1972 жылы оқшауланған және содан бері оны медициналық және ғылыми зерттеулерде әлеуетті пайдалану үшін кеңінен зерттелді.РаналексинБревинин-1 пептидтік отбасының мүшесі, грам-оң және грам-теріс штаммдарды қоса алғанда, әртүрлі бактерияларға қарсы күшті екендігі анықталды.Раналексин әртүрлі ғылыми зерттеулерде қолдану мүмкіндігі үшін зерттелді.Қызығушылықтың бір саласы - оның микробқа қарсы белсенділігі, оның әртүрлі бактерия штаммдарына қарсы тиімді екендігі көрсетілген.Бұл оны антибиотиктерге төзімді бактериялармен күресу үшін жаңа антибиотиктерді әзірлеуге перспективалы үміткер етеді.
Техникалық сипаттамалар
Сыртқы түрі: ақ немесе ақ түсті ұнтақ
Тазалық (HPLC):≥98,0%
Бірыңғай қоспа:≤2,0%
Ацетат мазмұны (HPLC): 5,0%~12,0%
Судың құрамы (Карл Фишер):≤10,0%
Пептидтердің мазмұны:≥80,0%
Буып-түю және жөнелту: төмен температура, вакуумды орау, қажетінше мг-ға дейін дәл.
Қалай тапсырыс беруге болады?
1. Contact us directly by phone or email: +86-13735575465, sales1@gotopbio.com.
2. Интернетте тапсырыс беріңіз.Онлайн тапсырыс формасын толтырыңыз.
3. Пептид атауын, CAS нөмірін немесе ретін, қажет болса тазалығын және модификациясын, санын және т.б. көрсетіңіз. Біз 2 сағат ішінде баға ұсынысын береміз.
4. Тиісті түрде қол қойылған сатып алу-сату шарты және NDA (жария етпеу туралы келісім) немесе құпия келісім бойынша тапсырыс сәйкестендіру.
5. Біз тапсырыс барысын уақытында үнемі жаңартып отырамыз.
6. Жүкпен бірге DHL, Fedex немесе басқалары арқылы пептидті жеткізу және HPLC, MS, COA қамтамасыз етіледі.
7. Сапамызда немесе қызметімізде қандай да бір сәйкессіздік болса, ақшаны қайтару саясаты орындалады.
8. Сатудан кейінгі қызмет: Егер біздің клиенттерде эксперимент кезінде пептид туралы сұрақтар туындаса, бізбен байланысыңыз, біз оған қысқа мерзімде жауап береміз.
Компанияның барлық өнімдері тек ғылыми-зерттеу мақсатында пайдаланылады, ол'кез келген тұлғалардың адам ағзасына тікелей қолданылуына тыйым салынады.
Жиі қойылатын сұрақтар:
Құрамында Cys бар пептидтер жөнелту алдында азайған ба?
Егер пептидтің тотығуы анықталмаса, біз әдетте Cys-ті төмендетпейміз.Барлық полипептидтер рН2 жағдайында тазартылған және лиофилденген шикі өнімдерден алынады, бұл кем дегенде белгілі бір дәрежеде Cys тотығуын болдырмайды.Құрамында Cys бар пептидтер pH6,8 деңгейінде тазартуға нақты себеп болмаса, рН2 деңгейінде тазартылады.Егер тазарту pH6,8 деңгейінде орындалса, тазартылған өнімді тотығуды болдырмау үшін дереу қышқылмен өңдеу керек.Сапаны бақылаудың соңғы сатысында құрамында Cys бар пептидтер үшін, егер MS картасында молекулалық салмақ (2P+H) затының болуы табылса, бұл димердің пайда болғанын көрсетеді.Егер MS және HPLC проблемасы болмаса, біз тікелей лиофилизациялаймыз және тауарларды әрі қарай өңдеусіз жөнелтеміз.Айта кету керек, құрамында Cys бар пептидтер уақыт өте баяу тотығудан өтеді, ал тотығу дәрежесі пептидтердің реттілігіне және сақтау шарттарына байланысты.
Пептидтің ілмектелгенін қалай анықтауға болады?
Сақина түзілуінің аяқталғанын тексеру үшін Эллман реакциясын қолданамыз.Эллман сынағы оң болса (сары), сақина реакциясы толық емес.Сынақ нәтижелері теріс (сары емес) болса, сақина реакциясы аяқталды.Біз өз клиенттерімізге циклизацияны анықтаудың талдау есебін бермейміз.Жалпы, QC есебінде Эллманның сынақ нәтижелерінің сипаттамасы болады.
Маған триптофан бар циклдік пептид керек, ол тотыға ма?
Триптофанның тотығуы пептидтердің тотығуында жиі кездесетін құбылыс болып табылады және пептидтер әдетте тазартудан бұрын циклденеді.Триптофанның тотығуы орын алса, HPLC бағанында пептидтің сақталуы уақыты өзгереді, ал тотығуды тазарту арқылы жоюға болады.Сонымен қатар, тотыққан пептидтерді MS арқылы анықтауға болады.
Пептид пен бояғыштың арасына саңылау қою керек пе?
Егер сіз пептидке үлкен молекуланы (бояғыш сияқты) қосатын болсаңыз, пептид пен лигандтың арасына пептидтің өзін қатпарлау немесе бүктеу арқылы рецепторға кедергіні азайту үшін бос орын қойған дұрыс. оның конъюгаты.Басқалары аралықтарды қаламайды.Мысалы, белоктардың қатпарлануында белгілі бір жерге флуоресцентті бояғышты қосу арқылы амин қышқылының қатпарлы құрылымы бір-бірінен қаншалықты қашықтықта орналасқанын анықтауға болады.
N терминалында биотин модификациясын жасағыңыз келсе, биотин мен пептидтер тізбегі арасында бос орын қою керек пе?
Біздің компания қолданатын стандартты биотинді таңбалау процедурасы пептид тізбегіне Ahx, содан кейін биотин қосу болып табылады.Ahx - пептид пен биотин арасындағы тосқауыл ретінде әрекет ететін 6 көміртекті қосылыс.
Фосфорланған пептидтердің дизайны бойынша кеңес бере аласыз ба?
Ұзындық ұлғайған сайын байланыстыру тиімділігі фосфорланған амин қышқылынан бастап біртіндеп төмендейді.Синтез бағыты C терминалынан N терминалына дейін.Фосфорланған амин қышқылынан кейінгі қалдық 10-нан аспауы керек, яғни N терминалынан С терминалына дейінгі фосфорланған амин қышқылына дейінгі аминқышқылдарының қалдықтарының саны 10-нан аспауы керек.
Неліктен n-терминалды ацетилдену және С-терминал амидациясы қажет?
Бұл модификациялар пептидтің ыдырауын болдырмайды және пептидке бастапқы ақуыздағы альфа-амин және карбоксил топтарының бастапқы күйіне еліктеуге мүмкіндік береді.